心肌梗死后室间隔穿孔的外科治疗
薛松 胡振雷 徐根兴 黄日太 刘沙 连锋 谢波
【摘要】目的 急性心肌梗死后室间隔穿孔是一种严重的并发症,死亡率很高。本研究通过回顾总结急性心肌梗死后室间隔穿孔的外科治疗经验,探讨如何提高此类疾病的疗效。方法 自2004年1月至2009年12月,12例急性心梗合并室间隔穿孔的患者接受了手术治疗,平均65.3±6.8岁,其中男性10例,女性2例。前室间隔穿孔5例(41.7%),后室间隔穿孔7例(58.3%)。合并冠状动脉单支病变2例(16.7%),2支病变6例(50%),3支病变4例(33.3%)手术距室间隔穿孔发生时间间隔为1-26日,平均为15.3±8.6日。手术采用David方法。随访时间6-55月,平均28.5±20.9月。结果 1例手术当天因无法控制的左室壁出血死亡,一例术后第二天死于无法纠正的低心排,围术期死亡率16.7%。随访过程中1例术后7个月猝死,原因不明,1例术后47个月因再次心梗,心源性休克死亡。最终存活8例(80%)。术后并发症:因出血再次开胸止血2例,频发室性心律失常2例,房颤3例,肾功能不全1例,肺部感染3例,伤口愈合不良再次缝合1例。术后呼吸辅助时间76.8±28.9小时,术后ICU 时间7.5±3.8天。全组无1例术后室缺再通。结论 急性心梗后室间隔穿孔是一种死亡率极高的疾病,外科手术是目前唯一有效的干预手段。合适的手术方式,积极的围术期治疗能够取得较好的临床效果,挽救患者生命。
【关键词】 心肌梗死 室间隔穿孔 冠心病
The outcome of surgical repair for postinfarction ventricular rupture
【Abstract】 Objective Ventricular septal defect (VSD) is one of the most serious and life-threatening complications of acute myocardial infarction. The aim of this study was to evaluate the results of the patients after surgical repair of postinfarction VSD. Methods A total of 12 consecutive patients (mean age, 65.3±6.8 years) underwent postinfarction VSD repair using a standardized technique in our department. A retrospective analysis of clinical and operative data and long-term survival was performed. The localization of VSD was posterior in 58.3% and anterior in 41.7% of the patients. Results The hospital mortality was 16.7% (2 patients). The causes of hospital death wwere persistent low cardiac output and bleeding of left ventricular incision respectively. The actuarial survival rate of in-hospital survivors during follow up years was 80% . Conclusions The surgical repair of postinfarction VSD is feasible and sufficient . Adequate operative technique and efficient preoperative treatment may improve the surgical results.
室间隔穿孔是一种继发于急性心肌梗死的严重并发症。其病理为心室前壁或下壁心肌梗死累及室间隔,室间隔心肌细胞透壁性坏死,在左右心室的压差下心室血流发生左向右分流,导致严重的血流动力学紊乱,心功能恶化。在急性心梗患者中,其发生率为1%-2%。室间隔穿孔一旦发生,若不行有效干预,三周内死亡率极高。多数患者因心源性休克无法逆转而死亡。外科手术是目前治疗此类疾病,挽救生命的有效手段。我科自2004年1月至2009年12月为12例急性心梗,室间隔穿孔患者进行了手术治疗,占同期冠心病手术的0.18%。现进行回顾性研究总结。
对象和方法:
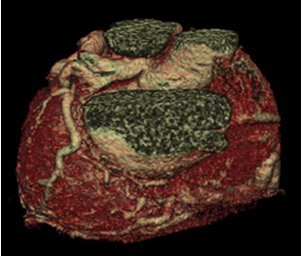
患者一般资料:自2004年1月至2009年12月,12例急性心梗合并室间隔穿孔的患者接受了手术治疗,其中男性10例,女性2例,年龄为55岁—73岁,平均65.3±6.8岁。所有患者术前均行冠状动脉造影,心脏超声,心电图,心肌酶谱检查,明确诊断。前室间隔穿孔5例(41.7%),后室间隔穿孔7例(58.3%)合并冠状动脉单支病变2例(16.7%),2支病变6例(50%),3支病变4例(33.3%)。术前4例合并左心功能衰竭,肺水肿,低氧血症,须利尿,扩血管,正性肌力药物持续注入,主动脉球囊反搏辅助治疗。本组患者术前合并高血压8例,糖尿病6例,高脂血症3例,肾功能不全2例,陈旧性心梗1例,二尖瓣轻度返流2例。术前左室射血分数48.6±12.3%。8例发病3周后手术,4例因血流动力学不稳定,行急诊手术。术前行PTCA+支架植入术4例。手术距室间隔穿孔发生时间间隔为1-26日,平均为15.3±8.6日。
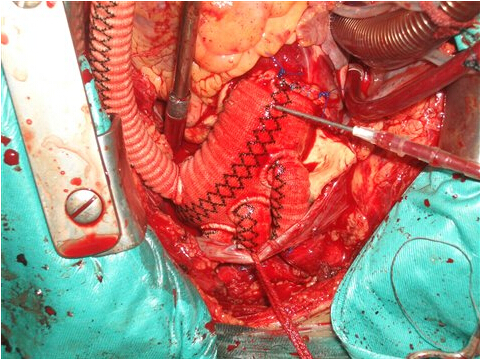
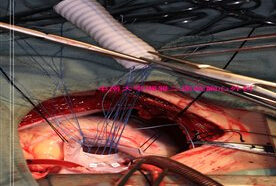
手术方法:手术均在全麻体外循环下进行。胸骨正中切口暴露心脏,在左室表面仔细探查,辨别梗塞区。心脏灌注停跳液后在梗塞区心室肌最薄弱处切开心室壁。前壁心梗合并前室间隔穿孔的患者中,心室切口位于左室前壁近心尖部,冠状动脉左前降支左侧1-2cm处,确定室间隔穿孔的位置及梗塞心肌的范围,若梗塞心肌组织已明显纤维化,比较坚韧,则按照室间隔缺损大小裁剪涤纶补片,用4-0 prolene线将补片连续缝合于缺损边缘纤维组织,覆盖缺损。若梗塞区组织脆弱,尚未纤维化,则采用David方法,裁剪一约4*6大小涤纶补片,将补片缝合于室间隔及心室游离壁的健康心肌组织上,把梗塞区心肌以及室间隔缺损区域隔离在左室腔以外。最后用毛毡条及1-0 prolene缝线“三明治法”关闭左室切口。下壁心梗合并后室间隔穿孔的患者中,心室切口位于左室下壁中部,冠状动脉后降支左侧1-2cm处,可分别向心尖部及二尖瓣瓣环侧延伸。缺损往往位于后室间隔远端靠近左室下壁处,若缺损周围组织坚韧,则将涤纶补片及纤维组织连续缝合修补缺损。若组织脆弱,采用David方法,将一三角形涤纶补片缝合覆盖于后乳头肌根部,左室下壁正常心肌组织及二尖瓣瓣环纤维组织上,将下壁心梗区和室间隔穿孔处与左室腔分隔开。心室切口关闭方法如前述。所有患者均同期对病变冠状动脉进行了完全再血管化,左前降支用乳内动脉搭桥,其余病变冠脉用自体静脉作桥血管材料。搭桥1-3支,平均1.9±0.7支。术中主动脉阻断时间为69.3±19.7min,体外循环时间为126.2±34.2min。
围术期处理:全组12例术后早期均须正性肌力药物(多巴胺2-10μg/kg/min,肾上腺素0.01-0.1μg/kg/min)维持治疗,5例因术后低心排予以IABP辅助,根据Swan-Ganz导管监测的肺毛细血管契压调整体循环容量,积极利尿,术后早期尿量少于1ml/kg/h者在容量补足的前提下予静脉推注速尿或静脉持续泵入速尿,及时纠正电解质及酸碱平衡紊乱。室性心律失常者予以利多卡因或可达龙静脉注入,同时维持血钾浓度4.5mmol/l以上。房颤者予以静脉持续注入可达龙以控制心室率及复律。积极抗感染治疗,痰培养阳性者根据药物敏感试验使用抗菌素。加强营养支持及体疗。术后若无活动性出血征象则及早使用抗凝药物。
患者随访:采用门诊或电话方式随访。随访时间6-55月,平均28.5±20.9月。
结果:
全组12例中1例手术当天因无法控制的左室壁出血死亡,一例术后第二天死于无法控制的低心排,围术期死亡率16.7%。10例康复出院。随访过程中1例术后7个月猝死,原因不明,1例术后47个月因再次心梗,心源性休克死亡。最终存活8例(80%)。术后并发症:因出血再次开胸止血2例,频发室性心律失常2例,房颤3例,肾功能不全1例,肺部感染3例,伤口愈合不良再次缝合1例。术后呼吸辅助时间76.8±28.9小时,术后ICU 时间7.5±3.8天。全组无1例术后室缺再通。
讨论:
1957年Cooly及其同事首先报道了急性心梗后室间隔穿孔的手术治疗(1),此后很多外科医生尝试各种手术方法,希望可以降低居高不下的手术死亡率。1977年Deggett运用人工材料替代坏死心肌组织,使得手术死亡率明显下降(2)。1987年,David发表文章介绍其用涤纶片将左室成形,并把室间隔穿孔区及梗死心肌均隔离于左室腔外,这样在解决左向右分流的同时保留了左室的几何构型,避免左室重构及室壁瘤的形成,手术效果非常满意(3)。本组6例室间隔穿孔3周后患者因梗死心肌明显纤维化,用补片直接修补缺损。另6例采用David手术方法,其中包括4例因血流动力学不稳定而急诊手术者,2例死亡,死亡率33.3%,与其他中心的结果类似,但高于David报道的19%,原因可能是这6例患者病情偏重。死亡病例均为术前血流动力学不稳定者,其中1例术前合并肾功能不全。本组总体手术死亡率较低(16.7%),可能是因为多数患者手术距穿孔发生3周以上(66.7%),病情趋于稳定,梗死心肌组织已被纤维组织替代,此阶段手术风险较低。但这么理想的手术时机并非一定能够等到,相当一部分患者在等待中心脏功能恶化,多器官功能衰竭,故不应一味等待,一旦低心排症状无法改善,应果断手术,效果优于保守治疗。
有文献报道后室间隔穿孔是手术高死亡率的危险因素之一,主要原因是此类缺损往往较难显露,也不易于修补操作。Moor指出右心功能的损害及右心室压的增加是造成死亡率上升的原因(4)。本组中后室间隔穿孔者死亡1例,死亡率14.3%,并不比前室间隔穿孔者死亡率高。David手术方法使得后室间隔缺损易于与左室隔开,同时对右室的干扰减至最低,可能是手术效果改善的原因。
多数文献均指出术前血流动力学不稳定者,尤其是心源性休克,IABP辅助效果不佳者,术后早期死亡率高(5-7)。本组4例中2例死亡,占50%,印证了这一点。与手术早期死亡相关的因素还有术前二尖瓣返流,高龄,正性肌力药物依赖,术中体外循环时间过长等(8)。本组因病例数较少,未作相关危险因素的分析。
术前及术后IABP辅助在本组治疗中作用至关重要,无论是术前循环的维持还是术后低心排的改善,都需要IABP的参与。IABP可以增加冠状动脉的灌注,改善心肌氧供,减轻左室后负荷,减少心肌氧耗,稳定循环状况。本组术后5例须IABP辅助,其中1例因肾功能衰竭死亡,其余4例恢复良好。术前IABP辅助有可能减少左向右分流,从而改善心功能,降低手术死亡率,有报道认为在术前不存在心源性休克的室间隔穿孔患者中,IABP辅助者术后死亡率显著低于未用者(9)。
是否在处理室间隔穿孔的同时对非梗塞区的病变冠状动脉进行再血管化是长期以来外科医生争论的话题。室间隔穿孔患者病情危重,保守治疗死亡率很高,相当一部分患者须急诊手术,因此有时来不及或无法承受冠状动脉造影检查。手术中冠状动脉再血管化也增加了主动脉阻断时间和体外循环时间,可能会增加术后并发症发生率。但另一方面,冠状动脉完全再血管化也许可以改善此类患者的远期预后。
Jeppsson等发现在早期死亡率方面,搭桥组和非搭桥组没有显著性差异,但是冠脉吻合口的数量是术后死亡的独立危险因素,这可能是因为吻合口数量代表了冠脉病变的弥散程度(10)。Barker等研究发现经统计学矫正的术后4年的生存率方面,同期搭桥的患者明显优于未搭桥者(11)。Labrousse指出同期行搭桥手术可降低近期死亡率,因此须在处理室间隔缺损同时对狭窄冠脉进行旁路手术,改善心肌血供(8)。Cox用多变量分析的统计学方法发现不完全的冠脉再血管化是重要的死亡危险因素,在预测术后死亡率方面仅次于室间隔穿孔残余漏(12)。Muehrcke的研究表明相对于后室间隔穿孔,前室间隔穿孔患者同期行冠脉搭桥效果更为明显(13)。
另外一些学者的研究得出了阴性或相反的结果。如Deja等用Cox回归模型未能得出令人信服的证据支持同期搭桥手术(14)。Parry认为,在重症病人中,虽然同期搭桥可以改善心肌血供,但因此造成的体外循环时间延长抵消了其积极作用,所以他们的统计结果为阴性(15)。Held指出体外循环时间的延长是手术死亡的独立预测因素(16)。
虽然观点各异,但多数学者的研究结果支持修补室间隔穿孔的同时行冠状动脉完全再血管化,而肺梗塞区狭窄冠脉的旁路移植可以通过侧枝循环改善梗塞区的心肌血供,从而改善远期预后。本组所有患者均同期行搭桥手术,随访28.5±20.9月,存活率80%。取得了良好的临床效果。
室间隔穿孔修补后再通是此类手术常见的问题,文献显示发生率为10%-40%。Deja的报道中44%发生术后再通,30%须再次手术,9%再通者死亡。因此手术方式很重要(14)。Labrousse等采用双层补片修补室缺,未发现残余漏(8)。本组无术后残余漏,临床效果佳,究其原因,一方面是一部分患者心肌组织已经纤维化,较坚韧,另一方面是采取了David手术方法。
本组例数较少,为回顾性的病例总结分析,因此有一定的缺陷,有待进一步收集病例,进行深入统计分析。
结论:
急性心梗后室间隔穿孔是一种死亡率极高的疾病,外科手术是目前唯一有效的干预手段。合适的手术方式,积极的围术期治疗能够取得较好的临床效果,挽救患者生命。
参考文献
1. Cooley DA, Belmonte BA, Zeis LB, Schnur S. Surgical repair of ruptured interventricular septum following acute myocardial infarction. Surgery 1957;41:930 –7.
2. Dagett WM, Guyton RA, Mundth ED, et al. Surgery for post-myocardial infarct ventricular septal defect. Ann Surg 1977;186:260 –71.
3. David TE. Surgical treatment of postinfarction ventricular septal rupture. Aust J Thorac Cardiovasc Surg 1992;1:7–10.
4. Moore CA, Nygaard TW, Kaiser DL, Cooper AA, Gibson RS.Postinfarction ventricular septal rupture: the importance of location of infarction and right ventricular function in determining survival. Circulation 1986;74:45–55.
5. Dalrymple-Hay MJ, Monro JL, Livesey SA, Lamb RK. Postinfarction ventricular septal rupture: the Wessex experience. Semin Thorac Cardiovasc Surg 1998;10:111– 6.
6. Labrousse L, Choukroun E, Chevalier JM, et al. Surgery for post infarction ventricular septal defect (VSD): risk factors for hospital death and long term results. Eur J Cardiothorac Surg 2002;21:725–32.
7. David TE, Armstrong S. Surgical repair of postinfarction ventricular septal defect by infarct exclusion. Semin Thorac Cardiovasc Surg 1998;10:105–10.
8.Labrousse L, Choukroun E, Chevalier JM, Madonna F, Robertie F. Surgery for post infarction ventricular septal defect (VSD): risk factors for hospital death and long term results. Eur J Cardiothorac
Surg 2002;21:725–31.
9.Long-Term Results After Surgical Repair of Postinfarction Ventricular Septal Rupture by Infarct
Exclusion Technique Nestoras Papadopoulos, MD, Anton Moritz, MD, PhD, Omer Dzemali, MD, et al.Ann Thorac Surg 2009;87:1421–5)
10.Jeppsson A, Liden H, Johnsson P, Hartford M, Ra?degran K. Surgical repair of post infarction ventricular septal defects: a national experience. Eur J Cardiothorac Surg 2005;27:216–221.
11.Barker TA, Ramnarine IR, Woo EB, et al. Repair of post-infarct ventricular septal defect with or without coronary artery bypass grafting in the northwest of England: a 5-year multi-institutional experience. Eur J Cardiothorac Surg 2003;24:940–946.
12.Cox FF, Plokker HW, Morshuis WJ,et al. Importance of coronary revascularization for late survival after postinfarction ventricular septal rupture. A reason to perform coronary angiography prior to surgery. Eur Heart J 1996;17:1841–1845.
13. Muehrcke DD, Daggett WM Jr, Buckley MJ, et al. Postinfarct ventricular septal defect repair:effect of coronary artery bypass grafting. Ann Thorac Surg 1992;54:876–882.
14.Deja MA, Szostek J, Widenka K, Szafron B, Spyt TJ, Hickey MS, Sosnowski AW. Post infarction ventricular septal defect – can we do better? Eur J Cardiothorac Surg 2000;18:194–201.
15..Parry G, Goudevenos J, Adams PC, Reid DS. Septal rupture after myocardial infarction: is very early surgery really worthwhile? Eur Heart J 1992;13:373–382.
16. Held AC, Cole PL, Lipton B, Gore JM, Antman EM, Hockman JS, Corrao J, Goldberg RJ, Alpert JS. Rupture of the interventricular septum complicating acute myocardial infarction: a multicenter analysis of clinical findings and outcome. Am Heart J 1988;116(5 Pt 1):1330–1336.
君健网www.junjian99.com独家刊登,如需转载请注明出处并保留完整信息。
260例冠脉搭桥术的临床分析 上一篇 | 下一篇 先天性心脏病合并感染性心内膜炎肺...
- 经胸右室穿刺封堵婴儿室间隔缺损25例报告2014-12-15
- 风湿性心脏病瓣膜置换术后焦虑与抑郁状况分析2014-12-10
- 高海拔地区59例双瓣膜置换术的临床分析2014-12-10
- 肺动脉夹层动脉瘤综述2014-12-15
- 马凡综合征主动脉根部瘤的改良Bentall术治疗2014-12-15
- 深低温停循环后梯度灌注复温脑保护的实验研究2014-12-15
- 组织工程血管基质的制备及保存2014-12-15
- 胸腔镜下体外循环心脏手术10例报道2014-12-15
- 原位心脏移植患者术后远期随访与分析2014-12-15
- 全球首个在“移植子宫”内孕育的婴儿降生2014-12-10
-
医生姓名:刘伏友
所在科室:肾内科
工作医院:中南大学湘雅二医院
专业职称:主任医师
擅长疾病: 腹膜透析、各类肾病、慢性肾功能衰竭、尿毒症、血液...